Анализ влияния на бюджет
- Методология /
-
5940
В РФ ежегодно утверждается ПГГ бесплатного оказания гражданам медицинской помощи за счёт государственных источников финансирования. Источниками финансирования ПГГ являются средства:
- федерального бюджета;
- бюджетов субъектов РФ;
- бюджетов местного самоуправления;
- Фонда обязательного медицинского страхования.
Согласно статье 80 Федерального закона РФ от 21.11.2011 г. № 323-ФЗ (ред. от 03.07.2016 г.) «Об основах охраны здоровья граждан РФ» в рамках ПГГ осуществляется обеспечение ЛП, входящими в Перечень ЖНВЛП [1].
В постановлении Правительства РФ от 28.08.2014 г. № 871 «Об утверждении правил формирования перечней лекарственных препаратов для медицинского применения и минимального ассортимента лекарственных препаратов, необходимых для оказания медицинской помощи» анализ влияния на бюджет является одним из основных видов экономического анализа, результаты которого представляются в Комиссию Минздрава РФ в качестве обоснования включения препаратов в ограничительные Перечни [2].
Анализ влияния на бюджет (АВБ, англ. budget impact analysis (BIA)) – это метод экономического исследования, основной целью которого является оценка финансовых последствий (прямых медицинских затрат – расходов системы здравоохранения) включения анализируемых лекарственных препаратов в Перечни лекарственных препаратов для медицинского применения, формируемые в рамках реализации Программы государственных гарантий.
Ключевые элементы АВБ включают в себя: оценку размера целевой популяции, терапии; анализ прямых медицинских затрат в текущей медицинской практике, а также изменения в прямых медицинских затратах после возможного внедрения нового ЛП в клиническую практику (ожидаемой клинической практики) (рис. 1) [3]. При проведении АВБ учитываются результаты анализа безопасности и эффективности ЛП, влияющие на прямые медицинские затраты в государственной системе здравоохранения [4].
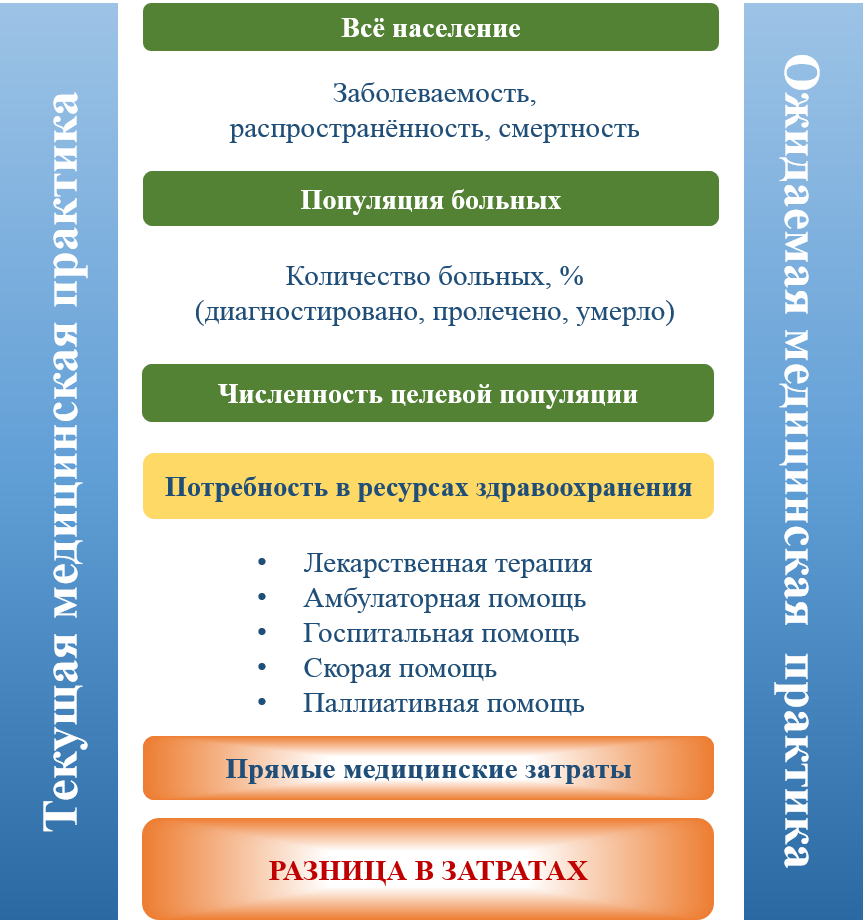
Рис. 1. Ключевые элементы анализа влияния на бюджет
Определение цели исследования. Основная цель проведения АБВ – это оценка возможных финансовых последствий включения ЛП в Перечни с учётом изменения частоты использования уже включённых в эти Перечни ЛП, в рамках реализации ПГГ [4].
Определение условий применения. Должны быть определены условия оказания медицинской помощи для применения ЛП, так как от них зависят источники финансирования:
- амбулаторные – из федерального бюджета и бюджетов субъектов РФ;
- дневной стационар – из федерального бюджета, бюджета субъектов РФ и средств системы ОМС;
- круглосуточный стационар – из федерального бюджета, бюджета субъектов РФ и средств системы ОМС;
- скорая медицинская помощь – из федерального бюджета, бюджетов субъектов РФ и средств системы ОМС.
Определение целевой популяции. Проведение АВБ основывается на характеристике и численности целевой популяции пациентов, которую необходимо описать [4].
Популяция, включаемая в АВБ, должна состоять из пациентов, соответствующих показаниям применения нового ЛП в течение временного горизонта моделирования. Далее следует отразить все запланированные ограничения на использование ЛП, особенности внедрения в клиническую практику, применение ЛП у ранее не лечившихся пациентов [5].
Целевая популяция является «открытой» в том плане, что субъекты могут включаться и исключаться по ходу исследования, в зависимости от их текущего соответствия критериям включения (например, при изменении показаний, появлении ограничений к терапии, исчезновении симптомов, смерти). Если частоты входа и выхода из модели стабильны и одинаковы, размер целевой популяции не будет изменяться со временем. Однако изменения будут происходить, если новый ЛП увеличит продолжительность терапии, замедлит прогрессирование болезни или снизит смертность, при этом не устраняя состояние/заболевание. Например, если критерием включения является «умеренная тяжесть заболевания», а новый ЛП замедляет прогрессирование заболевания, то целевая популяция начнёт увеличиваться на фоне проводимой терапии. Схема АВБ должна учитывать влияние этих изменений на размер исследуемой популяции [5].
Также важно учесть пропорцию, которую занимают представители целевой популяции в определённых подгруппах населения, разделённых по тяжести или стадии заболевания, по наличию и характеру сопутствующих заболеваний, по возрасту, полу, национальности, группе риска и другим важным характеристикам. Учитываться должны те подгруппы, в которых влияние нового ЛП на бюджет здравоохранения окажется отличным от общей популяции. Особенно важно включить поправку на подгруппы в схему АВБ в том случае, если новый ЛП может изменить пропорции целевых субъектов в подгруппах [5].
Когда размер популяции с интересующим нас состоянием/заболеванием будет оценён, необходимо оценить долю пациентов с диагностированным заболеванием, долю получающих терапию, а также распределение по степени тяжести заболевания. Всё это подразумевает использование строгих критериев включения для оценки количества больных, соответствующих критериям целевой популяции. Исследователю важно оценить не только текущий размер целевой популяции и структуру тяжести заболевания, но и то, как эти оценки будут изменяться на протяжении моделируемого отрезка времени без или с внедрением нового ЛП [5].
Эти изменения могут влиять на бюджет здравоохранения и, по возможности, должны быть учтены в модели на основании результатов РКИ или из регистров. Кроме того, на основе имеющихся литературных данных или мнения экспертов должно быть учтено любое диагностическое исследование, которое может способствовать увеличению целевой популяции за счёт улучшения диагностики или более точного определения степени тяжести болезни [5].
При оценке АВБ нового ЛП для терапии хронических состояний в течение первых нескольких лет после его внедрения будет иметь место «эффект навёрстывания». Например, если новый ЛП показан тем, кто ранее безуспешно получал специфическую терапию хронического заболевания, то в каждом моделируемом году в целевой популяции придётся учитывать две группы пациентов: тех, кто только что закончил безуспешную стандартную терапию и перешёл на новую, и тех, кто закончил стандартную терапию раньше (год или более года назад) и уже изменил своё лечение либо на исследуемый ЛП, либо на какое-то ещё лечение, которое снова может оказаться менее эффективным, чем изучаемый ЛП (группа «навёрстывания») [5].
Чтобы эффективно включать в модель АВБ новых пациентов и пациентов из группы «навёрстывания», должна быть получена релевантная информация из эпидемиологических исследований по размеру каждой группы пациентов, соответствующей критериям включения [5].
Таким образом, при построении математической модели АВБ (АВБ-калькулятора в MS Excel, описание которого см. ниже) необходимо учесть ежегодный прирост пациентов из-за рождаемости и заболеваемости, а также улучшения диагностики и убыль из-за выздоровления, либо смерти, или перевода пациента на другую схему лечения из-за непереносимости, неэффективности лечения, развития резистентности или НЯ.
Источниками информации о численности пациентов в целевой популяции могут быть:
- регистры пациентов / заболеваний;
- федеральное государственное и отраслевое статистическое наблюдение;
- результаты отечественных и зарубежных эпидемиологических исследований;
- экспертная оценка.
Построение модели на гипотетической группе недопустимо.
Определение временного горизонта. АВБ должен быть представлен в рамках адекватного промежутка времени в соответствии с бюджетным периодом [5].
Временной горизонт АВБ должен быть выбран в соответствии с принятым способом формирования бюджета здравоохранения РФ с точки зрения краткосрочной и долгосрочной перспективы: годовой бюджет здравоохранения и 3-летний период представляют собой плановый период для реализации многоэтапных целевых программ, в том числе и ПГГ бесплатного оказания гражданам медицинской помощи. Согласно рекомендациям [4], временной горизонт АВБ должен составлять от 1 до 5 лет; отдельно представляются результаты за первый год применения ЛП.
Горизонт моделирования за пределами пяти лет требует множественных допущений, он может понадобиться, чтобы проиллюстрировать уменьшение затрат на лечение болезней, которые могут наступить уже после прекращения применения изучаемого ЛП. Например, лечение хронического вирусного гепатита (ХВГ) предотвращает развитие цирроза или рака печени, которые являются вероятными событиями в отдалённом будущем после окончания терапии ХВГ [5].
Оценка влияния на медицинскую практику. Как правило, АВБ сравнивает сценарии, включающие целый ряд медицинских вмешательств. Первым следует оценить сценарий использования текущей медицинской практики в целевой популяции (стандартную терапию). Одним из вариантов стандартной терапии может являться отсутствие каких-либо медицинских вмешательств или паллиативная помощь [5].
В случае, если ЛП предлагается к включению в:
- Перечень ЖНВЛП, текущая практика лекарственной терапии включает в себя только препараты, включённые в Перечень ЖНВЛП;
- Перечень ОНЛС, текущая практика лекарственной терапии включает в себя только препараты, включённые в Перечень ОНЛС;
- Перечень дорогостоящих лекарственных препаратов, текущая практика лекарственной терапии включает в себя только препараты, включённые в Перечень дорогостоящих лекарственных препаратов.
Источники информации, на основании которых определена текущая практика должны быть представлены.
Аналитическая схема АВБ должна учитывать вариативность в некоторых частотных и стоимостных параметрах. Если для назначения ЛП требуется проведение диагностических исследований, их частоту и стоимость также следует включить в схему анализа [5].
Внедрение нового ЛП приводит в движение различные рыночные процессы, включающие замену ЛП и возможное расширение фармацевтического рынка. Во время проведения АВБ достоверно неизвестно, будет ли новый ЛП внедрён на рынок и какой эффект он окажет на существующие на данный момент терапевтические подходы, поэтому следует предусмотреть три варианта возможного внедрения ЛП [5]:
- новый ЛП будет добавлен к списку уже применяемых методов лечения (дополнение);
- новый ЛП вытеснит один или несколько существующих ЛП (замена);
- новый ЛП сможет быть использован в ситуациях, в которых на данных момент не существует эффективного лечения, а есть только поддерживающая терапия, или у пациентов, которые прекратили или отказались от использования доступных методов лечения по причине их неэффективности, непереносимости, развития НЯ или по любым другим причинам (нет аналогов).
Эти виды внедрения ЛП могут иметь отношение к различным популяционным подгруппам, и их распределение может изменяться с течением времени. Иными словами, изменения не происходят мгновенно, как только новый ЛП попадает на рынок, поэтому прогнозы таких изменений являются сложным, но очень важным компонентом АВБ [5].
Изменения имеют различное значение для Комиссии Минздрава РФ:
- дополнение к существующей лекарственной терапии приведёт к появлению дополнительных затрат, включая вероятные добавочные стоимости из-за изменений в профиле безопасности ЛП при их комбинации [5];
- расширение применения ЛП увеличит затраты на лекарственную терапию, но это может быть скомпенсировано за счёт терапии ранее неизлечимых пациентов [5];
- при замене стоимость новых ЛП может быть частично возмещена благодаря сокращению применения диагностических и лабораторных методов исследования [5].
Внедрение в практику новых ЛП и их влияние на стандартный набор применяемых медицинских процедур являются ключевыми компонентами АВБ [5].
Анализ должен быть прозрачным по отношению к допущениям, касающимся стандартной терапии и изменений, ожидаемых при внедрении в практику новых ЛП [5].
Таким образом, необходимо описать текущую и ожидаемую (моделируемую) клиническую практику лечения при включении ЛП в Перечни [4]:
- «дополнительная альтернатива» – при включении не предполагается исключения из практики ранее включённых в Перечни ЛП, часть пациентов перейдёт на лечение новым ЛП (%);
- «замена» – включение предполагает исключение из практики ранее включённых в Перечни ЛП; необходимо указывать препараты исключения и долю пациентов (%), которая перейдёт на лечение новым ЛП;
- «нет аналогов» – подаваемый для включения ЛП является новым методом лечения и не имеет аналогов.
При определении текущей практики терапии изучаемого показания (заболевания или состояния) указывается перечень ЛП и частота их назначения (табл. 1) [4].
Таблица 1. Текущая практика лекарственной терапии целевой популяции пациентов с учётом условий оказания медицинской помощи
|
№ |
МНН |
Частота назначения ЛП (от 1 до 100 %) |
|
1 |
|
|
|
2 |
|
|
|
… |
|
|
|
ИТОГО: |
100 % |
|
Если в Перечне ЖНВЛП нет ЛП с такими же показаниями, то могут рассматриваться и не включённые в Перечень ЖНВЛП препараты, при этом изучаемый вами ЛП должен расцениваться как дополнительная альтернатива к текущей практике [4].
Если в РФ вообще не зарегистрированы ЛП с такими же показаниями, то рассматриваемый препарат также расценивается как дополнительная альтернатива к текущей практике [4].
Ожидаемая (моделируемая) схема лечения зависит как от скорости внедрения в практику нового ЛП, так и от меры замещения или расширения с его помощью методов стандартной терапии (текущей практики). Скорость внедрения в клиническую практику нового ЛП изменяется по мере того, как врачи и пациенты знакомятся с ним [5].
Существует два способа оценки уровня внедрения новых ЛП в схемы лечения [5]:
- использование оценки ожидаемой удельной доли производителя на рынке;
- экстраполирование опыта внедрения ЛП с такими же показаниями.
С помощью этих подходов необходимо определить, будет ли новый ЛП добавлен к стандартной терапии или он заменит её частично или целиком [5].
Исследование фармацевтического рынка, оценка производителя и мнение независимых экспертов являются рекомендованными источниками информации для оценки уменьшения использования стандартной терапии, когда новый ЛП станет доступным [5].
Частоту назначения лекарственных препаратов и их наименования в текущей и ожидаемой клинической практике можно взять из:
- стандартов медицинской помощи;
- федеральных клинических рекомендаций;
- фармакоэпидемиологических исследований [6];
- исследований потребления ЛП [7];
- регистров больных / заболеваний;
- маркетинговых исследований для выявления доли распределения ЛП в реальной клинической практике и основных трендов в схемах лечения;
- данных государственных закупок ЛП;
- анализа истории болезни и амбулаторных карт;
- экспертных оценок (с представлением количества экспертов, их специальности, указанием регионов, времени проведения оценки).
Смоделированная (ожидаемая) практика лекарственной терапии с учётом вероятной частоты назначения нового ЛП должна быть описана. Частота назначения ЛП может принимать значения от 1 до 100 % целевой популяции, а сумма частот не должна превышать 100 %. Если у изучаемого ЛП нет аналогов по данному показанию, то частота его назначения определяется как 100 % целевой популяции (см. табл. 2) [4].
Таблица 2. Ожидаемая (моделируемая) практика лекарственной терапии целевой популяции пациентов с учётом условий оказания медицинской помощи
|
№ |
МНН |
Частота назначения ЛП (от 1 до 100 %) по годам временного горизонта |
||||
|
1-й год |
2-й год |
3-й год |
4-й год |
5-й год |
||
|
1. |
|
|
|
|
|
|
|
2. |
|
|
|
|
|
|
|
… |
|
|
|
|
|
|
|
ИТОГО: |
100 % |
100 % |
100 % |
100 % |
100 % |
|
Расчёт прямых медицинских затрат. Внедрение новых ЛП в клиническую практику может привести к изменению симптомов, длительности, исходов или же темпа прогрессирования болезни и, соответственно, к изменению объёма терапевтических вмешательств. Однако включение в расчёты прямых медицинских затрат определённых патологических состояний может потребовать использования значительных допущений и ненужного увеличения горизонта моделирования. В АВБ, совмещённом с клинико-экономическим исследованием, эти оценки можно получить из самого КЭА. Исходя из вышесказанного, если доступны качественные входные данные и рассматриваемые изменения действительно имеют влияние на бюджет здравоохранения, то их следует включить в АВБ. И если такое решение будет принято, то модель должна быть составлена таким образом, чтобы пользователь мог увидеть результаты как с учётом влияния этих изменений на бюджет, так и без них [5].
В некоторых случаях терапия вносит изменения в организацию медицинской помощи (например, дни, проведённые в стационаре, посещения врача на дому) и, таким образом, в пропускную возможность системы здравоохранения. Но в то же время эти изменения могут не приводить к изменениям в прямых медицинских затратах, так как сама система здравоохранения не всегда может финансово приспособиться к новым условиям в течение рассчитываемого промежутка времени (например, персонал не может быть сокращён или переведён на другие должности). Тем не менее по-прежнему желательно включить влияние нового ЛП на изменения в медицинском обслуживании, так как это может привести к определённым выводам при планировании бюджета здравоохранения и без учёта влияния на бюджет [5].
Таким образом, расчёт прямых медицинских затрат в текущей клинической практике и в моделируемой должен учитывать затраты на ЛП (их указывают отдельно), а также затраты на:
- применение специальных устройств для введения препарата;
- лабораторные методы исследований, таких как генетическое тестирование, терапевтический лекарственный мониторинг и др.;
- лечение нежелательных явлений;
- специфические диагностические методы исследований;
- реабилитационные мероприятия;
- профилактические мероприятия;
- манипуляции и процедуры, оказываемые медицинскими работниками на дому.
АВБ должен использовать данные, отражающие прямые медицинские затраты, специфичные для конкретной целевой популяции, и учитывать любые ожидаемые изменения [5]. Расчёт затрат на текущий и ожидаемый вариант терапии должен проводиться на каждый год в рамках установленного временного горизонта (от 1 до 5 лет) [4].
Затраты на текущий (табл. 3) и ожидаемый (моделируемый) (табл. 4) вариант лекарственной терапии рассчитываются по следующей формуле:
Cost(P)=Cost(1)×F(Th)×P, где
Cost(P) – стоимость лекарственной терапии целевой популяции больных, руб.;
Cost(1) – стоимость лекарственной терапии в год на одного больного, руб.;
F(Th) – частота назначения лекарственного препарата;
P – количество больных в целевой популяции, чел.
Таблица 3. Затраты на лекарственную терапию целевой популяции в текущей практике
|
№ |
Международное непатентованное название |
Средневзвешенные затраты на 1 пациента в год, руб. |
Количество пациентов, чел. |
Затраты на текущий вариант лекарственной терапии, руб. |
|
1. |
|
|
|
|
|
2. |
|
|
|
|
|
... |
|
|
|
|
|
ИТОГО: |
|
|
|
|
Таблица 4. Затраты на лекарственную терапию целевой популяции в ожидаемой практике
|
Год проведения АВБ |_____| (1, 2, … 5-й) |
||||
|
№ |
Международное непатентованное название |
Средневзвешенные затраты на 1 пациента в год, руб. |
Количество пациентов, чел. |
Затраты на ожидаемый вариант лекарственной терапии, руб. |
|
1. |
|
|
|
|
|
2. |
|
|
|
|
|
... |
|
|
|
|
|
ИТОГО: |
|
|
|
|
Результаты. Результаты АВБ представляются в виде разницы в прямых медицинских затратах (в абсолютных и/или относительных показателях) между текущей практикой лекарственной терапии и ожидаемой практикой с учётом включения рассматриваемого ЛП в ограничительные Перечни за указанный временной горизонт [4].
Абсолютная разница влияния на бюджет между текущей и ожидаемой практикой терапии рассчитывается по следующей формуле:
BIA(cd)= Cost(P)1-Cost(P)0, где
BIA(cd) – абсолютная разница в суммарных затратах между текущим вариантом лекарственной терапии и ожидаемым (с использованием исследуемого ЛП), руб.;
Cost(P)0 – текущая стоимость терапии всех пациентов при базовом распределении, руб.;
Cost(P)1 – ожидаемая стоимость терапии при потенциальном увеличении количества пациентов, использующих изучаемый ЛП, руб.
Следует отдельно указать разницу в затратах на лекарственную терапию, а также на общие прямые медицинские затраты [4]. Макет оформления таблиц по расчёту разницы в прямых медицинских затратах в текущей и ожидаемой клинической практике за указанный временной горизонт с разбивкой по годам по каждому показанию представлен в табл. 5 и 6.
Таблица 5. Разница в затратах на лекарственное лечение целевой популяции в текущей и ожидаемой практике
|
Год проведения АВБ |_____| (1, 2, … 5-й) |
|||
|
Показание к назначению |
Затраты на текущий вариант лекарственной терапии, руб. |
Затраты на ожидаемый вариант лекарственной терапии, руб. |
Разница затрат на лекарственную терапию, руб. |
|
1. |
|
|
|
|
2. |
|
|
|
|
… |
|
|
|
|
ИТОГО: |
|
|
|
Таблица 6. Разница в прямых медицинских затратах на оказание медицинской помощи целевой популяции в текущей и ожидаемой практике
|
Год проведения АВБ |_____| (1, 2, … 5-й) |
|||
|
Показание к назначению |
Прямые медицинские затраты с учётом текущего варианта лекарственной терапии, руб. |
Прямые медицинские затраты с учётом ожидаемого варианта лекарственной терапии, руб. |
Разница в прямых медицинских затратах, руб. |
|
1. |
|
|
|
|
2. |
|
|
|
|
… |
|
|
|
|
ИТОГО: |
|
|
|
Относительная разница влияния на бюджет между текущей и ожидаемой практикой терапии рассчитывается по следующей формуле:
BIA(rd)= Cost(P)1÷Cost(P)0-1, где
BIA(rd) – относительная разница в суммарных затратах между текущим вариантом лекарственной терапии и ожидаемым (с использованием исследуемого ЛП), %;
Cost(P)0 – текущая стоимость терапии всех пациентов при базовом распределении, руб.;
Cost(P)1 – ожидаемая стоимость терапии при потенциальном увеличении количества пациентов, использующих изучаемый ЛП, руб.
Изменения параметров со временем. Некоторые параметры АВБ могут изменяться со временем. К этим параметрам относятся:
- стоимость медицинских услуг;
- появление нового вида терапии в клинических рекомендациях или стандартах;
- изменение цен на ЛП (например, в связи с истечением срока действия патента на оригинальный препарат и появлением генериков);
- изменения в определении/классификации болезни, показаниях и методах терапии.
Прогнозирование этих изменений достаточно сложно, но для указанного в АВБ промежутка времени подобные попытки всё же должны быть осуществлены, при условии, что эти допущения прозрачны, обоснованы и соответствуют известным данным [5].
Дисконтирование. В клинико-экономическим анализе дисконтирование затрат является обязательным. Однако этот подход не рекомендуется для АВБ, где интересы плательщика состоят в определении ожидаемого влияния в каждый конкретный момент времени. Таким образом, АВБ должен представлять данные по финансовым потокам в каждый бюджетный период без дисконтирования [5].
Анализ чувствительности. Важно, чтобы схема АВБ позволяла пользователям просчитать в том числе альтернативные варианты результатов внедрения ЛП и их влияние на применение стандартной терапии [5]. Для АВБ имеет значение неопределённость двух типов:
- неопределённость параметров, рассчитанных на основе входных данных (оценка эффективности стандартной и новой терапии);
- неопределённость структуры модели, представленная допущениями, принятыми при создании модели АВБ (ожидаемые изменения в схемах лечения при внедрении нового ЛП или ожидаемые ограничения по его внедрению).
Область значений (диапазоны), используемую в анализе неопределённости, можно получить из обзоров опубликованных исследований. Использование произвольных диапазонов, таких как ±20 % или ±50 %, не рекомендуется, так как они не отражают фактическую неопределённость параметров [5].
Так как информация по многим параметрам ограничена, бо́льшая часть неопределённости параметров в АВБ не может быть достоверно рассчитана, и, таким образом, стандартные подходы, такие как однофакторный, многофакторный и вероятностный анализы чувствительности, не могут быть проведены в полном объёме. Бо́льшая же часть неопределённости является структурной, и параметризировать её нелегко. По этим причинам следует создать правдоподобные альтернативные сценарии, изменяя определённые входные параметры и структурные допущения [5]. Обязательно необходимо рассмотреть альтернативные сценарии при изменении таких параметров, как численность целевой популяции или численность (доля) пациентов, получающих предлагаемый ЛП и цены на ЛП [4].
Если в анализе сценария учитывается влияние приверженности пациентов лечению, то на основе исследования баз данных и проспективных исследований должны быть сделаны необходимые допущения. АВБ также должен оценивать влияние приверженности лечению на его эффективность и безопасность. Если не существует опубликованных данных о взаимосвязи приверженности лечению с результатами лечения, то возможно использовать альтернативные источники информации, например данные о фармакокинетике или фармакодинамике препарата или же мнение экспертов [5].
Валидация. Математическая модель и входные данные, используемые в АВБ, должны быть достоверными (валидными), чтобы обеспечить Комиссию Минздрава РФ надёжной информацией к моменту принятия ими решения о включении/невключении ЛП в ограничительные Перечни. Для этого при проведении АВБ необходимо произвести проверку правильности работы АВБ-калькулятора (описание см. ниже), включая все его формулы. В дополнение к этому, по возможности, следует сравнить адекватность оценок, выдаваемых моделью для первого года текущего варианта лекарственной терапии с уже имеющимися реальными данными [5].
Отчёт. Отчёт по проведённому АВБ должен быть структурирован и содержать следующие элементы.
Введение, которое должно кратко отразить современные подходы к лечению, эпидемиологическую информацию (распространённость, заболеваемость, смертность, тяжесть и склонность к прогрессированию, долю недиагностированных и нелеченых случаев, факторы риска, которые необходимо учитывать при оценке влияния на бюджет), количество пациентов с изучаемым заболеванием (целевую популяцию пациентов), описание эффективности и безопасности изучаемого ЛП, содержать гипотезу исследования, а также цели и задачи АВБ. Клинические данные должны включать в себя краткое описание подходящей под критерии включения популяции и существующие варианты лечения, их эффективность и безопасность, которые будут являться релевантными для АВБ.
Информация об экономическом влиянии должна включать в себя краткое описание предыдущих АВБ для изучаемого заболевания.
Методология. Отчёт должен определять дизайн АВБ (обычно это АВБ-калькулятор в MS Excel). В методологии должны быть обоснованы и описаны следующие разделы:
- позиция исследования;
- показания к применению ЛП;
- характеристики и численность целевой популяции пациентов;
- условия оказания медицинской помощи;
- текущая и ожидаемая медицинская практика;
- критерии эффективности и безопасности;
- препараты сравнения;
- временной горизонт;
- методы расчёта прямых медицинских затрат;
- методы проведения анализа чувствительности (альтернативных сценариев);
- структура АВБ-калькулятора.
Результаты. Следует включить в Отчёт графическое представление модели АВБ (см. рис. 2), которая облегчает для Комиссии Минздрава РФ понимание механизма подсчётов изменения затрат и ресурсов. В раздел описания схемы АВБ рекомендуется включить структурные диаграммы или другие визуальные изображения АВБ-калькулятора [5].
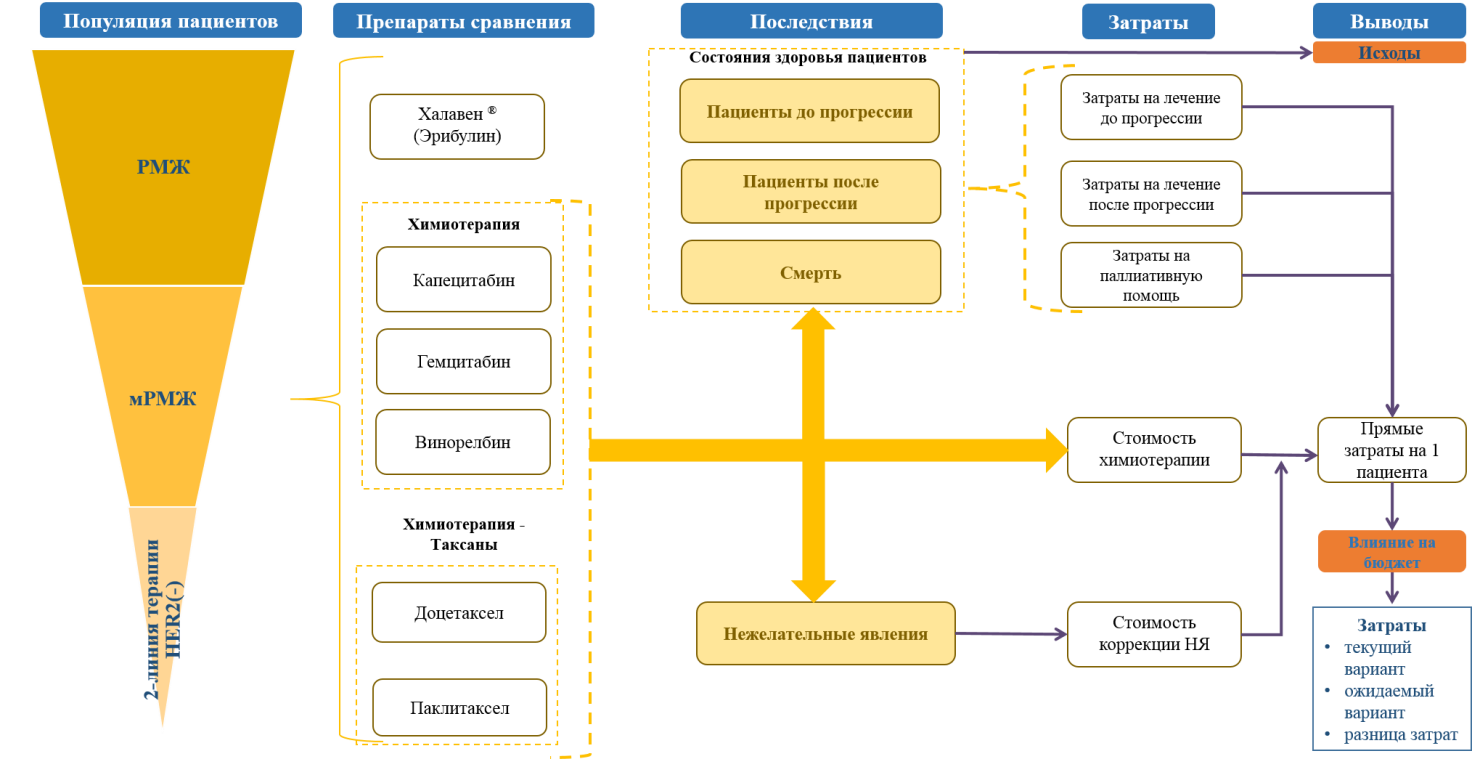
Рис. 2. Пример графического изображения модели анализа влияния на бюджет [8]
Примечания: РМЖ – рак молочной железы; мРМЖ – метастатический рак молочной железы; HER2 – рецептор фактора роста эпидермиса 2; HER2(-) – отрицательный статус опухоли; НЯ – нежелательные явления.
Должны быть представлены все входные значения, в том числе и для альтернативных сценариев, используемые в АВБ, уровень детализации должен быть достаточен для того, чтобы читатель мог воспроизвести все расчёты по модели самостоятельно. Источники входных данных должны быть детально описаны. Любые изменения или пересчёты показателей должны быть описаны достаточно детально, чтобы дать возможность их воспроизвести. Сильные и слабые стороны, ограничения, возможное направление и размер ошибки – всё должно быть отмечено. Должны быть обсуждены критерии выбора исследований и баз данных, являющихся источниками входной информации, а сами источники информации должны быть указаны в порядке появления в тексте. Все значения входных параметров и их источники должны быть представлены в виде таблиц. Методы и процесс сбора первичных данных, а также их адаптации для модели должны быть описаны и объяснены. Формы сбора данных или вопросники должны быть включены в Приложение к Отчёту [5].
Должно быть представлено описание расчётов, использованных при АВБ. Выбор всех представленных в результатах сценариев должен быть документирован и обоснован [5].
Все основные допущения должны быть представлены в табличной форме [5].
Результаты должны быть представлены детально с целью обеспечения гибкости при их использовании заинтересованными лицами. Влияние на бюджет должно быть представлено для каждого бюджетного периода в течение анализируемого промежутка времени; отдельно за первый год. Также должна быть предоставлена информация о затратах на ЛП и об использованных ресурсах за данный бюджетный период; отдельно затраты на ЛП за первый год. Оценки использования ресурсов должны быть отражены в таблице, показывающей изменения в их использовании для каждого подотчётного периода АВБ. Оценки использования ресурсов должны быть группированы по вмешательствам и по НЯ [5].
Все полученные результаты должны быть представлены в табличной и/или графической форме. Отдельная таблица должна показывать затраты на лекарственные препараты, общие прямые медицинские затраты и затраты по отдельным направлениям (ЛП, амбулаторное и стационарное лечение) для каждого отчётного периода. Также могут быть представлены изменения в ежегодных показателях результатов лечения. Всё это позволит обеспечить ясность для Комиссии Минздрава РФ, когда значительное влияние на бюджет здравоохранения будет сопровождаться не менее значительным положительным влиянием на здоровье пациентов [5].
Результаты анализа неопределённости (чувствительности) или анализа альтернативных сценариев должны быть описаны и обоснованы, представлены в виде диаграмм и таблиц. Торнадо-диаграммы, отображающие эффект изменения каждого из входящих в модель параметров в заданных диапазонах, должны быть включены в раздел, посвящённый результатам анализа сценариев [5].
В результатах должны быть описаны следующие разделы:
- показания к применению ЛП;
- характеристика и численность целевой популяции;
- условия оказания медицинской помощи;
- текущая и ожидаемая медицинская практика;
- показатели эффективности и безопасности ЛП;
- препараты сравнения;
- временной горизонт;
- прямые медицинские затраты и разница в прямых медицинских затратах (отдельно указать разницу затрат на лекарственную терапию);
- анализы неопределённости (чувствительности) или альтернативных сценариев.
Выводы. Необходимо обозначить основные выводы по основным результатам АВБ, которые должны содержать сведения о наличии или отсутствии необходимости выделения дополнительных средств (а возможно, и экономии средств бюджета здравоохранения) на реализацию ПГГ при включении ЛП в ограничительные Перечни [16]. Общий вывод по результатам АВБ должен быть следующим:
- Нужны дополнительные средства ___________ руб./год.
- Не нужны дополнительные средства.
- Экономия бюджета ПГГ ___________ руб./год.
Основные ограничения. Следует представить сведения об основных ограничениях в отношении ключевых вопросов, а именно – аспектов дизайна, включающих в себя применение в отсутствие показаний, допущения о несоблюдении рекомендаций, а также полноту и качество информации об исходных ресурсах и данных [5].
Заключение. Должно содержать краткое обсуждение основных результатов АВБ с выводом о наличии или отсутствии необходимости выделения дополнительных средств в случае включения нового ЛП в ограничительные Перечни [4].
Приложения могут включать:
- форму представления результатов исследования в Комиссию Минздрава РФ;
- анкету опроса экспертов (если применимо) с её описанием;
- опубликованную статью;
- математическую модель в виде АВБ-калькулятора в формате MS Excel
АВБ-калькулятор. АВБ требует достаточной гибкости для обеспечения оценок разными специалистами, поэтому важно, чтобы разработанный калькулятор на базе MS Excel позволял пользователям вносить их собственные значения затрат и целевой популяции. Программа также должна позволять пользователям с лёгкостью восстанавливать изначальные стандартные параметры; содержать простые в использовании таблицы. Все входящие параметры должны отображаться в виде одной или нескольких рабочих таблиц. Графы входных параметров должны быть обозначены различными цветами в зависимости от того, может ли пользователь вводить в них свои данные или нет. Выходные данные должны отображаться в одной или нескольких рабочих таблицах в логической манере, которая резюмирует все результаты, полученные пользователем [5]. Полезно использовать графическое изображение модели АВБ (см. рис. 2).
Если в АВБ-калькуляторе требуется ответить более чем на один анализируемый вопрос, то в таких случаях интерфейс пользователя должен быть спроектирован так, чтобы пользователь мог легко переключаться между различными вопросами [5].
Первый лист в MS Excel должен включать оглавление структуры модели, описание допущений и инструкцию к использованию модели. Все источники, вычисления и допущения, применимые к входным данным, должны быть отражены, должен быть приведён список всех использованных ссылок. Все расчёты должны быть доступны пользователю и представлены в полном объёме и включать подробное руководство для пользователей [5].
Также результаты моделирования АВБ должны быть представлены в формате, удобном для восприятия Комиссией Минздрава РФ, и быть приложены к Предложению на включение в ограничительные Перечни, при этом возможна разработка калькулятора только АВБ или клинико-экономического анализа совместно со «встроенным» АВБ. В готовом калькуляторе всегда должны представляться варианты различных ценовых категорий, которые можно произвольно включать или не включать в анализ, например учитывать только затраты на ЛП без других прямых медицинских затрат [5].
_________
Источник: Включение лекарственных препаратов в ограничительные перечни: пошаговый алгоритм / под общ. ред. Белоусова Д. Ю., Зырянова С. К., Колбина А. С. — М. : Издательство ОКИ : Буки Веди, 2019. — 252 с. : ил. ISBN 978-5-4465-2555-3. https://clck.ru/MBP84
_________
Литература
- Федеральный закон от 21.11.2011 № 323-ФЗ (ред. от 03.07.2016) «Об основах охраны здоровья граждан в Российской Федерации» (с изм. и доп., вступ. в силу с 01.01.2017) [Электронный ресурс]. – Режим доступа: https://clck.ru/DNwu9
- Постановление Правительства РФ от 28.08.2014 № 871 «Об утверждении правил формирования перечней лекарственных препаратов для медицинского применения и минимального ассортимента лекарственных препаратов, необходимых для оказания медицинской помощи» (в редакции постановлений Правительства РФ от 12.06.2017 № 700, от 29.10.2018 № 1283, от 20.11.2018 № 1390) [Электронный ресурс]. – Режим доступа: https://clck.ru/FwwBc
- Приказ Министерства здравоохранения Российской Федерации от 15.03.2019 № 18н «О внесении изменений в Положение о комиссии Министерства здравоохранения Российской Федерации по формированию перечней лекарственных препаратов для медицинского применения и минимального ассортимента лекарственных препаратов, необходимых для оказания медицинской помощи, утверждённое приказом Министерства здравоохранения Российской Федерации от 9 сентября 2014 г. № 498н» [Электронный ресурс]. – Режим доступа: https://clck.ru/GBJK2
- Методические рекомендации по оценке влияния на бюджет в рамках реализации Программы государственных гарантий бесплатного оказания гражданам медицинской помощи. Утверждены приказом ФГБУ «ЦЭККМП» Минздрава России от 23.12.2016 № 145-од [Электронный ресурс]. – Режим доступа: https://clck.ru/ETmvV
- Sullivan S. D., Mauskopf J. A., Augustovski F., et al. Principles of good practice for budget impact analysis II: Report of the ISPOR Task Force on Good Research Practices – Budget Impact Analysis [Электронный ресурс] // Value Health. – 2014. – № 17. – С. 5–14. – Режим доступа: https://clck.ru/HLDJ7
- Белоусов Д. Ю., Чеберда А. Е. Фармакоэпидемиологические исследования: методология и регулирование [Электронный ресурс] // Качественная клиническая практика. – 2017. – № 1. – С. 34–41. – Режим доступа: https://clck.ru/GHPic
- Чеберда А. Е. Исследования потребления лекарственных средств [Электронный ресурс] // Качественная клиническая практика. – 2017. – № 1. – С. 42–45. – Режим доступа: https://clck.ru/GHPi8
- Зырянов С. К., Белоусов Д. Ю. Анализ «влияния на бюджет» эрибулина у пациентов с метастатическим раком молочной железы [Электронный ресурс] // Качественная клиническая практика. – 2015. – № 4. – С. 64–72. – Режим доступа: https://clck.ru/HYUFk
.png)