В России зарегистрирован препарат для лечения раннего HER2-положительного рака молочной железы
- Новости /
-
2802
- Министерство здравоохранения РФ одобрило новое показание к применению препарата трастузумаб эмтанзин.
- В клинических исследованиях препарат вдвое снизил риск рецидива при адъювантной терапии пациентов с ранним HER2-положительным раком молочной железы и инвазивной остаточной опухолью после неоадъювантной терапии таксаном и трастузумабом.
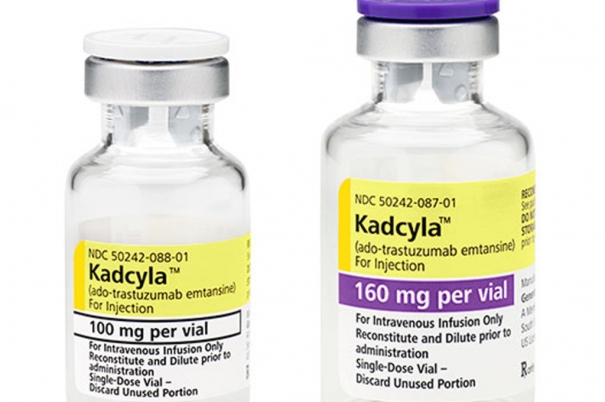
Компания «Рош» сообщает о регистрации в России нового показания к применению трастузумаба эмтанзина (торговое наименование Кадсила®). Препарат может быть назначен в качестве адъювантной терапии пациентов с ранним HER2-положительным раком молочной железы и инвазивной остаточной опухолью после неоадъювантной терапии таксаном и трастузумабом. Обновленная инструкция по применению трастузумаба эмтанзина одобрена Министерством здравоохранения РФ и опубликована на портале Государственного реестра лекарственных средств[1].
Новое показание основано на результатах исследования III фазы KATHERINE, которое показало, что трастузумаб эмтанзин на 50% снижает риск рецидива инвазивной злокачественной опухоли молочной железы или смерти от любой причины по сравнению c адъювантной терапией трастузумабом у пациентов с ранним HER2-положительным раком молочной железы с инвазивной остаточной опухолью после неоадъювантной терапии таксаном и трастузумабом[2].
По данным трехлетнего наблюдения в исследовании, у 88,3% пациентов, получавших трастузумаб эмтанзин, не было рецидива рака молочной железы по сравнению с 77% пациентов, получавших трастузумаб. Абсолютное улучшение составило 11,3%[3]. Прогноз у пациентов, имеющих остаточную опухоль после проведенной неоадьювантной терапии, хуже, чем у пациентов, достигших полного патоморфоза[4],[5].
«Одобрение нового показания к применению трастузумаба эмтанзина — это значительный прогресс в лечении HER2-положительного рака молочной железы в России, — говорит Екатерина Фадеева, медицинский директор АО «Рош-Москва». — Снижая риск рецидивов заболевания, врачи приближаются к заветной цели — добиться излечения для каждой пациентки с ранней стадией рака молочной железы».
Повышение шансов на излечение является главной задачей в терапии раннего HER2-положительного рака молочной железы, которая может включать применение лекарственной терапии до и после операционного вмешательства[6],[7]. Несмотря на достигнутый прогресс, у многих пациентов наблюдаются рецидивы заболевания в долгосрочной перспективе[8]. Неоадъювантную терапию проводят перед хирургическим вмешательством с целью уменьшения опухолевой массы и улучшения отдаленных результатов лечения и оценки чувствительности опухоли к проводимому лечению[9]. Адъювантная терапия проводится после операции и направлена на устранение оставшихся в организме опухолевых клеток, снижая тем самым риск рецидива онкологического заболевания[10].
Трастузумаб эмтанзин — это конъюгат моноклонального тела трастузумаб с химиопрепаратом эмтанзин, разработанный для доставки химиопрепарата непосредственно в HER2-положительные опухолевые клетки, потенциально ограничивая повреждение здоровых тканей[11],[12]. Препарат впервые зарегистрирован в России в 2015 году для применения в лечении HER2-положительного метастатического рака молочной железы[13].
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило заявку на регистрацию трастузумаба эмтанзина по нынешнему показанию в мае 2019 года, перед этим присвоив препарату статус «прорывной терапии», который призван ускорить разработку и исследования лекарственных средств для лечения опасных для жизни заболеваний[14].
Пресс-релиз
[1] Инструкция по медицинскому применению лекарственного препарата Кадсила®. Государственный реестр лекарственных средств, https://grls.rosminzdrav.ru/Default.aspx.. Доступ: 15.08.2019 г.
[2] Minckwitz G, et al. N Engl J Med. 2018; DOI: 10, 1056 / NEJMoa1814017.
[3] Там же.
[4] Cortazar P, et al. Lancet. 2014;384(9938):164-72.
[5] Gianni L, et al. Lancet. 2016;17(6):791-800.
[6] Scharl A, et al. Geburtshilfe Frauenheilkd. 2015; 75 (7): 683-91.
[7] Johns Hopkins Medicine. Neoadjuvant and Adjuvant Chemotherapy. http://www.hopkinsmedicine.org/breast_center/treatments_services/medical_oncology/neoadjuvant_adjuvant_chemotherapy.html.
[8] Slamon D, et al. BCIRG 006 trial. Presented at: SABCS; 2015 Dec 6-10; San Antonio, TX, USA. Abstract #S5-04.
[9] Johns Hopkins Medicine. Neoadjuvant and Adjuvant Chemotherapy. http://www.hopkinsmedicine.org/breast_center/treatments_services/medical_oncology/neoadjuvant_adjuvant_chemotherapy.html.
[10] Там же.
[11] Hurvitz SA, et al. J Clin Oncol. 2013;31(9):1157-63.
[12] Verma S, et al. N Engl J Med. 2012;367(19):1783-91.
[13] Инструкция по медицинскому применению лекарственного препарата Кадсила®. Государственный реестр лекарственных средств, https://grls.rosminzdrav.ru/Default.aspx. Доступ: 15.08.2019 г.
[14] US Food and Drug Administration. Breakthrough Therapy. [Internet; cited April 2019]. https://www.fda.gov/ForPatients/Approvals/Fast/ucm405397.htm.
.png)